Prolina
La prolina (Pro, P) o prolalina es uno de los aminoácidos que forman las proteínas de los seres vivos. En el ARN mensajero está codificada como CCU, CCC, CCA, CCG.
| Prolina | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Ácido pirrolidin-2-carboxílico | ||
| General | ||
| Símbolo químico | Pro, P | |
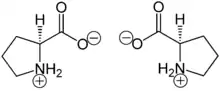
| Fórmula estructural |
 | |
| Fórmula molecular | C5H9NO2 | |
| Identificadores | ||
| Número CAS | 147-85-3[1] | |
| Número RTECS | TW3584000 | |
| ChEBI | 26271 | |
| ChEMBL | CHEMBL72275 | |
| ChemSpider | 594 | |
| DrugBank | DB00172 | |
| PubChem | 614 | |
| UNII | DCS9E77JPQ | |
| KEGG | C16435 | |
|
C1CCNC1C(=O)O
| ||
| Propiedades físicas | ||
| Masa molar | 115,13 g/mol | |
| Punto de fusión | 494 K (221 °C) | |
| Propiedades químicas | ||
| Acidez | 1,95; 10,47 pKa | |
| Familia | Aminoácido | |
| Esencial | No | |
| Codón | CCA, CCU, CCG, CCC | |
| Punto isoeléctrico (pH) | 6,3 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Se trata del único aminoácido proteinogénico cuya α-amina es una amina secundaria en lugar de una amina primaria. [cita requerida], pues su cadena lateral es cíclica y está compuesta por 3 unidades de metileno; estos quedan unidos al carbono alfa y al grupo amino, el cual pasa a llamarse imino.
La prolina se puede formar directamente a partir de la cadena pentacarbonada del ácido glutámico, y por tanto no es un aminoácido esencial.
Es una molécula que posee carga neta 0, por lo tanto es apolar pero no hidrófoba. Su masa molar es 115,13 g/mol.
Es un aminoácido apolar no aromático.
La prolina está involucrada en la producción del colágeno. Está también relacionada con la reparación y mantenimiento de los músculos y los huesos.
La prolina es la que confiere flexibilidad a la molécula de inmunoglobulina en la región de bisagra de esta.
La dirección del polipéptido está determinada por la prolina, si está en configuración cis o trans.[2]
Historia
Richard Willstätter obtuvo la prolina por vez primera en el laboratorio en 1900, mientras estudiaba la N-metilprolina. El año siguiente, Emil Fischer publicó la síntesis de la prolina mediante la hidrólisis de caseína con ácido hidroclórico.[3] El nombre prolina proviene de pirrolidina, uno de sus componentes.[4]
Referencias
- Número CAS
- «Péptidos. El enlace peptídico.». www.ehu.eus. Consultado el 28 de agosto de 2018.
- «Proline».
- «proline». American Heritage Dictionary of the English Language, 4.ª edición.