Isoxazolina
Las isoxazolinas son una clase de ectoparasiticidas de uso veterinario que se introdujeron por primera vez en Canadá en el año 2014, con los fármacos afoxolaner y fluralaner en forma de comprimidos. En un comienzo, su uso solo se autorizó para el tratamiento de pulgas y garrapatas en perros. Luego de estudios realizados, se sugirió que estos fármacos podrían ser efectivos frente a otros ectoparásitos, como los ácaros de la sarna (demodicosis por ejemplo).[1] [2] Posteriormente se amplió su uso en gatos.[3] [4] [5] Hasta julio del 2022, en el mercado se encuentran cuatro moléculas: lotilaner con el nombre comercial de Credelio de laboratorio Elanco[6], afoxolaner con el nombre comercial de Nexgard de laboratorio Merial[7], fluralaner con el nombre Bravecto[8] de laboratorio MSD y sarolaner como Simpárica[9] de laboratorio Zoetis.
| Isoxazolina | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
| 4,5-dihydro-1,2-oxazole | ||
| Identificadores | ||
| Número CAS | &Units=SI 504-73-4 | |
| PubChem | 12304501 | |
| DrugBank | DB11369 | |
| Datos químicos | ||
| Fórmula | C3H5NO | |
| Peso mol. | 71.08 g/mol | |
|
C1CON=C1
| ||
|
InChI=1S/C3H5NO/c1-2-4-5-3-1/h2H,1,3H2
Key: WEQPBCSPRXFQQS-UHFFFAOYSA-N | ||
| Sinónimos | 2-Isoxazoline, 4,5-dihydro-1,2-oxazole, 4,5-Dihydroisoxazole, Isoxazoline, 504-73-4, Isoxazole, UNII-NBB8G944P3, NBB8G944P3, DTXSID90486713 | |
| Farmacocinética | ||
| Biodisponibilidad | Rápida | |
| Unión proteica | 99 % | |
| Metabolismo | hepático | |
| Vida media | Entre 12 días y 4 semanas | |
| Excreción | renal y biliar | |
| Datos clínicos | ||
| Vías de adm. | Oral y spot-on | |
Descripción
Son compuestos heterocíclicos de cinco miembros y estructuralmente poseen un núcleo de fenilo heterocíclico sustituido con cloruro.[10] El anillo recibió el nombre según la nomenclatura de compuestos heterocíclicos. Son isómeros estructurales de las oxazolinas y existen en tres isómeros diferentes según la ubicación del doble enlace. Las isoxazolinas tienden a tener reacciones de apertura del anillo y su posterior reordenamiento debido a que el enlace N-O es relativamente débil. Los compuestos que contienen un anillo de isoxazolina tienen una variedad de usos y muchos son biológicamente activos. Según un estudio del año 2014,[11] las esponjas marinas producen varias isoxazolinas naturales, las cuales podrían tener actividad anticancerígena. Los compuestos nuevos contienen una isoxazolina no aromática y una cadena lateral extendida. Las isoxazolinas fluralaner, sarolaner y afoxolaner se distribuyen como mezclas racémicas del enantiómero R, el cual según diversos estudios, es activo y ramificado, sin efectos adversos conocidos hasta la fecha.[10]
Síntesis
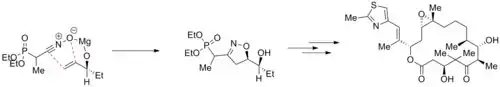
La síntesis de isoxazolinas 3,5-disustituídas ocurre a partir de cicloadiciones 1,3-dipolares de azúcares libres. Es uno de los métodos más importantes para la obtención de anillos heterocíclicos de cinco miembros. La síntesis no requiere condiciones enérgicas. Para aplicar estas cicloadiciones a la obtención de sistemas heterocíclicos nitrogenados-oxigenados, es necesario realizar la síntesis del dipolo óxido de nitrilo.[12]
Farmacocinética
Vías de administración
La administración de las isoxazolinas en gatos y perros es por vía oral y spot-on (pipeta),[13] [14] y en caso del sarolaner también intravenosa.[15]
Farmacocinética
En el caso del lotilaner luego de la administración oral, se absorbe rápidamente y tiene su pico de concentración en sangre en 2 horas. La ingestión de alimento al momento de la administración mejora su absorción. Tiene una vida media de aproximadamente 4 semanas, que proporciona una concentración en sangre efectiva que dura todo el intervalo entre dosis. La ruta de eliminación es por excreción biliar y renal (en menor proporción).[16]

El afoxolaner tiene una elevada absorción sistémica con una biodisponibilidad del 74 %. La concentración máxima media (Cmax) es de 1.655 ± 332 ng/ml en plasma entre las 2 y 4 horas de su administración. Su volumen de distribución en tejidos es de 2,6 ± 0,6 l/kg y el aclaramiento sistémico es de 5,0 ± 1,2 ml/h/kg. La vida media en sangre es de aproximadamente 2 semanas en la mayoría de los caninos, sin embargo puede haber diferencias entre razas o individuos. Se metaboliza en el perro en compuestos más hidrofílicos y luego se elimina. Se elimina mediante excreción urinaria y biliar. No se observa evidencia de ciclo enterohepático.[17]

El fluralaner también se absorbe rápidamente y alcanza concentraciones en sangre máximas en un día, mejorando su absorción con el alimento. Se distribuye sistémicamente y en tejido graso, hígado, riñón y músculo es donde tiene una mayor concentración. Tiene una persistencia prolongada y una lenta eliminación desde el plasma (t1/2 = 12 días). Además la falta de un metabolismo extenso hace que la concentración efectiva del fluralaner durante el intervalo entre dosis sea prolongada. Se observó variación individual en la Cmax y la t1/2. La principal vía de eliminación es en las heces donde se excreta inalterado (~90% de la dosis). También se elimina en menor proporción por orina.[18]

El sarolaner tiene una biodisponibilidad superior al 85%, sin embargo el consumo de alimento luego de la administración no afecta significativamente el grado de su absorción. El aclaramiento de sarolaner es bajo (0,12 ml/min/kg) y su volumen de distribución es moderado (2,81 l/kg). La vida media es de 12 días en el caso de administración intravenosa y 11 días en la administración oral, La unión a proteínas plasmáticas en pruebas in vitro fue de ≥99,9%. Los metabolitos resultantes se distribuyen ampliamente por los tejidos. Al igual que las moléculas precedentes, la principal ruta de excreción es la biliar y las heces.[19]

Farmacodinamia
Las Isoxazolinas actúan en los canales de cloro, particularmente en los canales GABA y glutamato, teniendo una selectividad mayor por las neuronas de los ácaros.[20] Se unen a un único y distinto lugar diana en los GABACls del insecto, bloqueando así los impulsos nerviosos pre y postsinápticos a través de las membranas celulares.[21] La hiper excitación prolongada produce una actividad incontrolada del sistema nervioso central, parálisis y posterior muerte de los parásitos.[22] Para que las isoxazolinas tengan efecto, las pulgas (C.felis y C.Canis) y garrapatas (Rhipicephalus sanguineus, Dermacentor reticulatus y Dermacentor variabilis, Ixodes ricinus e Ixodes scapularis, Amblyomma americanum y Haemaphysalis longicornis) deben alimentarse del animal.[23]
Interacciones
Ninguna conocida. Sin embargo al unirse a proteínas plasmáticas podrían competir con otras sustancias que tengan una acción similar como antiinflamatorios no esteroideos o aquellos derivados de cumarina.
Reacciones adversas
Las posibles reacciones adversas de las isoxalinas son: .[16] [17] [18] [19]
- Reacciones gastrointestinales como vómitos y diarreas
- Prurito
- Letargia
- Anorexia
- Signos neurológicos como convulsiones, ataxia y temblores musculares.
Han sido reportados casos de reacciones adversas en muy raras ocasiones y la mayoría fueron de resolución espontánea y transitorias. Sin embargo, la U.S. food & drug administration (FDA), reporto los potenciales efectos neurológicos con el uso de las isoxazolinas.[24]
En el caso del fluralaner quedado demostrada la seguridad del medicamento en perros reproductores, gestantes y lactantes.[18] En las otras moléculas, si bien estudios de laboratorio efectuados en ratas no han demostrado efectos teratogénicos o en la capacidad reproductiva de machos y hembras, la European Medicine Agency (EMA) informa que no quedó demostrada la inocuidad del medicamento veterinario durante la gestación, la lactancia o en perros reproductores.[25] [26] [27]
Especies de artrópodos afectadas
- Pulgas: Ctenocephalides felis y Ctenocephalides Canis.
- Garrapatas: Rhipicephalus sanguineus, Dermacentor reticulatus y Dermacentor variabilis, Ixodes ricinus e Ixodes scapularis, Amblyomma americanum y Haemaphysalis longicornis.[23]
- Ácaros: Demodex spp.,[28] Otodectes spp.,[29] Notoedres spp.[30]
Referencias
- Vincent E. Defalque (03/12/2021). «Uso de isoxazolinas para la demodicosis canina».
- Simpson, Andrew C (2021-01). «Successful treatment of otodemodicosis due to Demodex cati with sarolaner/selamectin topical solution in a cat». Journal of Feline Medicine and Surgery Open Reports (en inglés) 7 (1): 205511692098438. ISSN 2055-1169. doi:10.1177/2055116920984386. Consultado el 17 de agosto de 2022.
- Flores Ortega, Ariadna; Rey Sanchez, Nora Daniela (Marzo 2021). «Fluralaner: Explorando una molécula poco utilizada en gatos para el manejo de ectoparásitos.». Revista Vanguardia Veterinaria 18 (104): 14. ISSN 2007-557X.
- Bouza-Rapti, Pavlina; Tachmazidou, Anatoli; Farmaki, Rania (2022-01). «Effectiveness of a fluralaner spot-on formulation in a case of feline demodicosis due to Demodex cati». Journal of Feline Medicine and Surgery Open Reports (en inglés) 8 (1): 205511692110695. ISSN 2055-1169. PMC 8801658. PMID 35111330. doi:10.1177/20551169211069529. Consultado el 17 de agosto de 2022.
- Duangkaew, Lerpen; Hoffman, Heather (2018-06). «Efficacy of oral fluralaner for the treatment of Demodex gatoi in two shelter cats». Veterinary Dermatology (en inglés) 29 (3): 262-262. doi:10.1111/vde.12520. Consultado el 17 de agosto de 2022.
- «Elanco US». www.elanco.us. Consultado el 17 de agosto de 2022.
- «NexGard protege a tu perro de parásitos externos». nexgard.com.ar. Consultado el 16 de agosto de 2022.
- «Homepage». Entrada - Bravecto. Consultado el 16 de agosto de 2022.
- «¿Está tu perro a salvo de pulgas, garrapatas y ácaros (sarna)? ǀ Zoetis». Zoetis Pets (en lATAM-es). Consultado el 16 de agosto de 2022.
- Weber, Tina; Selzer, Paul M. (2016-02). «Isoxazolines: A Novel Chemotype Highly Effective on Ectoparasites». ChemMedChem (en inglés) 11 (3): 270-276. doi:10.1002/cmdc.201500516. Consultado el 11 de agosto de 2022.
- Kaur, Kamalneet; Kumar, Vinod; Sharma, Anil Kumar; Gupta, Girish Kumar (22 de abril de 2014). «Isoxazoline containing natural products as anticancer agents: A review». European Journal of Medicinal Chemistry (en inglés) 77: 121-133. ISSN 0223-5234. doi:10.1016/j.ejmech.2014.02.063. Consultado el 16 de agosto de 2022.
- Erik Larsen, Karl; Torssell, Kurt B. G. (1 de enero de 1984). «An improved procedure for the preparation of 2-isoxazolines». Tetrahedron (en inglés) 40 (15): 2985-2988. ISSN 0040-4020. doi:10.1016/S0040-4020(01)91313-4. Consultado el 16 de agosto de 2022.
- Bouza-Rapti, Pavlina; Tachmazidou, Anatoli; Farmaki, Rania (2022-01). «Effectiveness of a fluralaner spot-on formulation in a case of feline demodicosis due to Demodex cati». Journal of Feline Medicine and Surgery Open Reports (en inglés) 8 (1): 205511692110695. ISSN 2055-1169. PMC 8801658. PMID 35111330. doi:10.1177/20551169211069529. Consultado el 16 de agosto de 2022.
- Duangkaew, Lerpen; Larsuprom, Lawan; Anukkul, Pojnicha; Lekcharoensuk, Chalermpol; Chen, Charles (2018-06). «A field trial in Thailand of the efficacy of oral fluralaner for the treatment of dogs with generalized demodicosis». Veterinary Dermatology (en inglés) 29 (3): 208-e74. doi:10.1111/vde.12524. Consultado el 16 de agosto de 2022.
- «Ficha técnica de Simpárica».
- «Ficha técnica de Credelio».
- «Ficha técnica de Nextgard».
- «Ficha técnica de Bravecto».
- Taenzler, Janina; Wengenmayer, Christina; Williams, Heike; Fourie, Josephus; Zschiesche, Eva; Roepke, Rainer KA; Heckeroth, Anja R (2014-12). «Onset of activity of fluralaner (BRAVECTO™) against Ctenocephalides felis on dogs». Parasites & Vectors (en inglés) 7 (1): 567. ISSN 1756-3305. PMC 4263043. PMID 25471474. doi:10.1186/s13071-014-0567-6. Consultado el 11 de agosto de 2022.
- Lahm, George P.; Cordova, Daniel; Barry, James D.; Pahutski, Thomas F.; Smith, Ben K.; Long, Jeffrey K.; Benner, Eric A.; Holyoke, Caleb W. et al. (2013-05). «4-Azolylphenyl isoxazoline insecticides acting at the GABA gated chloride channel». Bioorganic & Medicinal Chemistry Letters (en inglés) 23 (10): 3001-3006. doi:10.1016/j.bmcl.2013.03.031. Consultado el 17 de agosto de 2022.
- Wengenmayer, Christina; Williams, Heike; Zschiesche, Eva; Moritz, Andreas; Langenstein, Judith; Roepke, Rainer KA; Heckeroth, Anja R (2014-12). «The speed of kill of fluralaner (Bravecto™) against Ixodes ricinus ticks on dogs». Parasites & Vectors (en inglés) 7 (1): 525. ISSN 1756-3305. PMC 4247686. PMID 25406442. doi:10.1186/s13071-014-0525-3. Consultado el 11 de agosto de 2022.
- «Ficha técnica del producto».
- Medicine, Center for Veterinary (4 de mayo de 2020). «Animal Drug Safety Communication: FDA Alerts Pet Owners and Veterinarians About Potential for Neurologic Adverse Events Associated with Certain Flea and Tick Products». FDA (en inglés). Consultado el 17 de agosto de 2022.
- «Veterinary medicine European public assessment report (EPAR): Simparica».
- «Veterinary medicine European public assessment report (EPAR): NexGard».
- «Veterinary medicine European public assessment report (EPAR): Credelio».
- Snyder, Daniel E.; Wiseman, Scott; Liebenberg, Julian E. (2017-12). «Efficacy of lotilaner (Credelio™), a novel oral isoxazoline against naturally occurring mange mite infestations in dogs caused by Demodex spp.». Parasites & Vectors (en inglés) 10 (1): 532. ISSN 1756-3305. PMC 5664441. PMID 29089049. doi:10.1186/s13071-017-2472-2. Consultado el 17 de agosto de 2022.
- Six, Robert H.; Becskei, Csilla; Mazaleski, Mark M.; Fourie, Josephus J.; Mahabir, Sean P.; Myers, Melanie R.; Slootmans, Nathalie (30 de mayo de 2016). «Efficacy of sarolaner, a novel oral isoxazoline, against two common mite infestations in dogs: Demodex spp. and Otodectes cynotis». Veterinary Parasitology. Special Issue: Sarolaner - A Novel Ectoparasiticide for Dogs. (en inglés) 222: 62-66. ISSN 0304-4017. doi:10.1016/j.vetpar.2016.02.027. Consultado el 17 de agosto de 2022.
- Curtis, Cathy F; Bourdeau, Patrick J; Barr, Philip Adam; Mukherjee, Rajat (2019-03). «Use of the novel ectoparasiticide fluralaner in the treatment of feline sarcoptic mange». Veterinary Record Case Reports (en inglés) 7 (1). ISSN 2052-6121. doi:10.1136/vetreccr-2018-000772. Consultado el 17 de agosto de 2022.
| Control de autoridades |
|
|---|
 Datos: Q65054682
Datos: Q65054682